ARTIGOS ORIGINAIS
INFLIXIMABE NA DOENÇA DE CROHN: EXPERIÊNCIA CLÍNICA DE UM CENTRO TERCIÁRIO PAULISTA
Infliximab in Crohn's Disease: Clinical Experience from a Single Tertiary Center of Sao Paulo State
Ulysses dos Santos Torres 1; Geni Satomi 2; Luiz SÉrgio Ronchi 2; JoÃo Gomes Netinho 3
1. Graduando em Medicina - Faculdade de Medicina de São José do Rio Preto (FAMERP); 2. Docentes da Disciplina de Coloproctologia da FAMERP; 3. Chefe da Disciplina de Coloproctologia da FAMERP; Doutor em Cirurgia pela Unicamp; Membro do Grupo de Estudos da Doença Inflamatória Intestinal no Brasil.
Resumo: Introdução: Na Doença de Crohn (DC) ocorre uma reatividade anormal dos linfócitos T da mucosa intestinal e produção excessiva de citocinas pró-inflamatórias, entre as quais o fator de necrose tumoral alfa (TNF-á). O infliximabe é um anticorpo monoclonal anti-TNF-á indicado no tratamento de pacientes com DC fistulizante ou não responsiva ao tratamento convencional. Objetivos: Caracterizar as indicações clínicas do infliximabe na DC em um serviço referencial paulista, avaliando padrões de resposta e a efetividade do tratamento através do Índice de Atividade da DC (CDAI). Pacientes e Métodos: O estudo foi observacional retrospectivo e analisou dados de 21 pacientes com DC em uso de infliximabe atendidos no Hospital de Base de Rio Preto entre janeiro de 2004 e julho de 2008. Resultados: Houve predomínio de pacientes do sexo feminino (67%), com média de idade de 33 anos. As indicações mais freqüentes foram fístulas perianais (48%). Resposta clínica total à droga ocorreu em 43% dos pacientes, e resposta parcial em 47%; a diferença da média do CDAI entre os grupos antes e após o tratamento foi de 244,61 pontos (p< 0,0005). Conclusões: O infliximabe induziu melhora clínica em 90% dos pacientes, acompanhada de redução da atividade da doença na avaliação através de um índice padronizado.
Descritores: Enteropatias Inflamatórias, Doença de Crohn, Fator de Necrose Tumoral alfa, Anticorpos Monoclonais, Evoluçăo Clínica.
INTRODUÇÃO
A Doença de Crohn (DC) é uma doença
inflamatória crônica do trato gastrointestinal, de etiologia
e patogênese ainda não inteiramente conhecidas. O
padrão etiopatogênico da doença inclui
suscetibilidade genética, desbalanço entre bactérias comuns
e patogênicas do trato intestinal, alterações na
integridade do epitélio intestinal e resposta imune
desregulada pela reatividade anormal dos linfócitos T da
mucosa intestinal, com produção excessiva de citocinas
pró-inflamatórias (1).
O fator de necrose tumoral alfa (TNF-?) é
uma citocina pró-inflamatória produzida sobretudo
por macrófagos ativados e linfócitos T, e atua no
recrutamento e ativação de células do sistema imune,
bem como na ativação de fibroblastos e células
endoteliais, com importante papel na atividade inflamatória
em mucosas (2).
Aprovado em 1998 nos EUA para o tratamento de formas moderadas a graves da DC, o
infliximabe é um anticorpo monoclonal IgG1 quimérico, 75%
humano e 25% murino, que se liga com elevada
afinidade ao TNF-?. As respostas propostas para sua ação
se dão não somente como consequência do bloqueio
direto do TNF-? solúvel ou transmembrânico, mas
também pela indução de apoptose de linfócitos T
(3), recuperação da barreira epitelial
(4), e indução da
motilidade dos fibroblastos intestinais, facilitando cicatrização
de lesões (5).
As indicações clínicas atuais em relação à
terapia biológica com infliximabe incluem doença
intestinal moderada ou grave em pacientes refratários ao
tratamento convencional, assim como a forma
fistulizante não responsiva ao tratamento cirúrgico
e/ou farmacológico convencional. Ainda não está claro,
também, se a abordagem com infliximabe seria mais
eficaz se precoce (top down approach), com
possíveis impactos benéficos sobre o curso natural da
doença, ou sendo indicada mais tardiamente, após a
ausência de resposta às drogas tradicionais
(step-up approach) (6). De qualquer maneira, nos últimos dez anos o
tratamento com infliximabe vem mostrando ser seguro
e trazendo resultados clínicos positivos entre os
pacientes que cumprem os critérios de indicação
(7).
O presente estudo teve por objetivo caracterizar as indicações clínicas do infliximabe em um
hospital-escola referencial no atendimento a pacientes
com DC no noroeste do estado de São Paulo, bem
como avaliar os padrões de resposta e a efetividade do
tratamento entre esses pacientes.
PACIENTES E MÉTODOS
O estudo foi observacional retrospectivo e analisou dados de prontuários de 21 pacientes com
DC atendidos no Ambulatório de Coloproctologia do
Hospital de Base da Faculdade de Medicina de São
José do Rio Preto (HB/ FAMERP), e que fizeram uso
de infliximabe entre janeiro de 2004 e julho de 2008.
A realização do estudo se deu somente
após aprovação pelo Comitê de Ética em Pesquisa da
mesma instituição, que dispensou a necessidade de
Termo de Consentimento Livre e Esclarecido em virtude
da metodologia da pesquisa.
Todos os pacientes receberam infusão endovenosa de infliximabe na dose de 5 mg/ kg,
em período variando de 2 a 4 horas, sob assistência
profissional especializada. O tratamento foi efetuado
seguindo o padrão de aplicação das doses nas semanas 0, 2 e
6, sucedendo-se doses de manutenção a cada 8
semanas.
Os pacientes foram analisados quanto ao sexo, idade, tempo de doença, sintomas presentes à data
de indicação do infliximabe, localização da doença
(com base em estudos anátomo-patológicos de
fragmentos colhidos por biópsia e em laudos de exames
de colonoscopia), histórico de cirurgias prévias
relacionadas à doença, indicações clínicas de uso do
medicamento, data da primeira aplicação e sua relação com
o tempo de evolução da doença, total de doses
infundidas individualmente, evolução clínica e escore de
classificação da doença antes e após as infusões da droga.
A evolução clínica foi considerada de
acordo com um dos três seguintes aspectos:
ausência de resposta ao infliximabe (ausência de melhora dos
sintomas intestinais e/ ou ausência de diminuição do
débito das fístulas); resposta parcial ao
infliximabe (diminuição considerável do débito das fístulas e/ ou
melhora considerável dos sintomas intestinais); e
resposta total ao infliximabe (interrupção total do débito
das fístulas e/ ou cicatrização dos trajetos fistulosos e/
ou fim dos sintomas intestinais). Para que se
obtivesse uma padronização adequada, considerou-se como
resposta obtida no pós-tratamento aquela registrada
em consulta realizada até 30 dias após a última
infusão, parâmetro que fornece mais claramente a
evolução clínica da doença à época da conclusão do
tratamento pela remissão, ou à época da última dose da
sequência de manutenção que vem levando ao controle da
doença ou à ausência de resposta.
Calculou-se o Índice de Atividade da
Doença de Crohn (CDAI, do inglês, Crohn's Disease
Activity Index) com base em dados registrados padronizadamente em prontuários durante o
atendimento ambulatorial de pacientes com DC que fazem
uso de infliximabe, em consultas realizadas até 30 dias
antes da primeira infusão do medicamento, assim
como naquelas realizadas em até 30 dias após a última
infusão, de acordo com a mesma padronização
estabelecida para a avaliação da evolução clínica. Em um
período de sete dias que antecedem a consulta marcada,
os pacientes em uso de infliximabe são instruídos a
registrar diariamente quatro das oito variáveis
necessárias para o cálculo do CDAI, quais sejam: número de
evacuações líquidas ou pastosas, intensidade da dor
abdominal, sensação de bem-estar geral e presença de
febre (esta última como um dos itens da variável
"complicações"). As outras quatro variáveis são
avaliadas clinicamente durante a consulta, assim como os
outros itens da variável "complicações", conforme será
discutido mais adiante.
Antes do início do tratamento, todos os
pacientes foram rotineiramente submetidos à realização
de radiografias torácicas e testes tuberculínicos, para
exclusão de possibilidade de tuberculose
(8). Além disso, todos os pacientes tiveram seguimento clínico
e laboratorial, antes e após as infusões, com
realização de hemogramas, testes de velocidade
de hemossedimentação, proteína C reativa, dosagem
de concentrações séricas de ferro, eletroforese de
proteínas no soro, bem como com avaliações
endoscópicas e radiológicas rotineiras.
A análise estatística dos dados foi
realizada através do software
Systat® 12 for Windows (Systat Software
Inc, 2007), sendo considerados
estatisticamente significantes valores p < 0,05. A
comparação entre as variáveis pareadas para análise da
diferença das médias do CDAI se realizou através do teste t
para amostras pareadas. A abordagem gráfica foi
realizada usando-se o desenho esquemático
(boxplot) de Tukey.
RESULTADOS
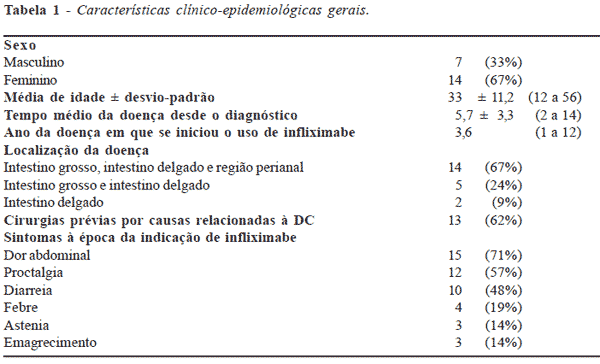
A distribuição dos pacientes segundo suas
características clínicas e epidemiológicas principais
encontra-se representada na tabela 1. Os sintomas mais
freqüentes à época da indicação do uso de infliximabe
foram dispostos em ordem decrescente, não se
considerando aqueles relacionados aos produtos de drenagem de
fístulas, que foram relatados pela totalidade dos pacientes com
a forma fistulizante da doença. Valores percentuais e
variações estão expressos entre parênteses.
 |
 |
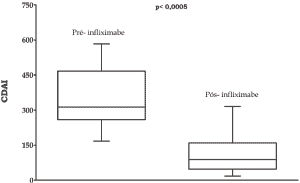 |
Gráfico 1 - Distribuição dos valores do CDAI da totalidade
dos pacientes antes e após o tratamento com infliximabe. |
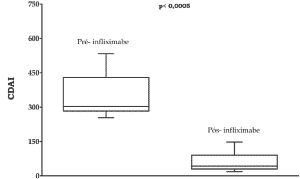 |
Gráfico 2 - Distribuição dos valores do CDAI antes e após
o tratamento entre o grupo de pacientes que clinicamente
obtiveram resposta total ao infliximabe. |
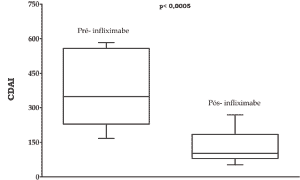 |
Gráfico 3 - Distribuição dos valores do CDAI antes e após
o tratamento entre o grupo de pacientes que clinicamente
obtiveram resposta parcial ao infliximabe. |
ABSTRACT: Introduction: In Crohn's Disease (CD) occurs an abnormal reactivity of T lymphocytes of intestinal mucosa and an exceeding production of proinflammatory cytokines, such as the tumor necrosis factor- alpha (TNF-á). Infliximab is a monoclonal antibody against TNF-á, indicated for treatment of patients with fistulizing or refractory CD. Objectives: To characterize the clinical indications of infliximab in CD at a referral center of Sao Paulo State, assessing patterns of response and treatment effectiveness by Crohn's Disease Activity Index (CDAI). Patients and Methods: This was an observational, retrospective study; data of 21 patients with CD receiving infliximab therapy at Hospital de Base de Rio Preto between January 2004 and July 2008 were analyzed. Results: Female patients were predominant (67%) and mean age was 33 years. Perianal fistulas represented the most common indication for infliximab use (48%). Complete clinical response to drug occurred in 43% of patients, and partial response in 47%; the mean difference of CDAI between the groups, before and after infliximab treatment, was 244.61 points (p< 0.0005). Conclusions: Infliximab induced clinical improvement in 90% of patients, with concomitant reduction of disease activity as measured by a standardized index.
Key words: Inflammatory enteropathy; Crohn's Disease; Tumor Necrosis Factor _alpha; Antibodies, Monoclonal; Clinical evolution.
Referências
1. Podolsky DK. Inflammatory Bowel Disease. N Eng J
Med 2002; 347(6):417-29.
2. Armstrong AM, Gardiner KR, Kirk SJ, Halliday MI,
Rowlands BJ. Tumour necrosis factor and inflammatory bowel
disease. Br J Surg. 1997; 84(8):1051_58.
3. Van den Brande JM, Braat H, van den Brink GR,
Versteeg HH, Bauer CA, Hoedemaeker I, et al. Infliximab but
not etanercept induces apoptosis in lamina propria
T-lymphocytes from patients with Crohn's disease. Gastroenterology.
2003; 124(7):1774_85.
4. Suenaert P, Bulteel V, Lemmens L, Noman M, Geypens
B, Van Assche G, et al. Anti-tumor necrosis factor
treatment restores the gut barrier in Crohn's disease. Am J
Gastroenterol. 2002; 97(8):2000_4.
5. Di Sabatino A, Pender S, Jackson C, Prothero J, Gordon
J, Picariello L, et al. Functional modulation of Crohn's
disease myofibroblasts by anti-TNF antibodies.
Gastroenterology. 2007; 133(1):137_149.
6. Oldenburg B, Hommes D. Biological therapies in
inflammatory bowel disease: top-down or bottom-up? Curr
Opin Gastroenterol. 2007; 23(4):395_9.
7. Blonski W, Lichtenstein GR. Safety of biologic
therapy. Inflamm Bowel Dis. 2007; 13(6):769-96.
8. Keane J, Gershon S, Wise RP, Mirabile-Levens E, Kasznica
J, Schwieterman WD, et al. Tuberculosis associated
with infliximab, a tumor necrosis factor alpha- neutralizing
agent. N Eng J Med. 2001; 345(15):1098- 104.
9. Kornbluth A. Infliximab approved for use in Crohn's
disease: a report on the FDA GI Advisory Committee
conference. Inflamm Bowel Dis. 1998; 4(4):328-9.
10. Targan SR, Hanauer SB, van Deventer SJ, Mayer L,
Present DH, Braakman T, et al. A short-term study of
chimeric monoclonal antibody cA2 to tumor necrosis factor alpha
for Crohn's disease. Crohn's Disease cA2 Study Group. N Engl
J Med 1997; 337(15):1029_35.
11. Present DH, Rutgeerts P, Targan S, Hanauer SB, Mayer
L, van Hogezand RA, et al. Infliximab for the treatment of
fistulas in patients with Crohn's disease. N Engl J Med
1999; 340(18):1398_405.
12. Hanauer SB, Feagan BG, Lichtenstein GR, Mayer LF,
Schreiber S, Colombel JF, et al. Maintenance infliximab for
Crohn's disease: the ACCENT I randomised trial. Lancet.
2002; 359(9317):1541_9.
13. Rutgeerts P, Feagan BG, Lichtenstein GR, Mayer LF,
Schreiber S, Colombel JF, et al. Comparison of scheduled and
episodic treatment strategies of infliximab in Crohn's
disease. Gastroenterology. 2004; 126(2):402_13.
14. Sands BE, Anderson FH, Bernstein CN, Chey WY,
Feagan BG, Fedorak RN, et al. Infliximab maintenance therapy
for fistulizing Crohn's disease. N Engl J Med. 2004;
350(9):876_85.
15. Wolters FL, Russel MG, Stockbrugger RW. Systematic
review: has disease outcome in Crohn's disease changed during
the last four decades? Aliment Pharmacol Ther. 2004;
20(5):483-96.
16. Nguyen GC, Tuskey A, Dassopoulos T, Harris ML,
Brant SR. Rising hospitalization rates for inflammatory
bowel disease in the United States between 1998 and 2004.
Inflamm Bowel Dis. 2007; 13(12):1529-35.
17. Faubion WA Jr, Loftus EV, Harmsen WS, Zinsmeister
AR, Sandborn WJ. The natural history of corticosteroid
therapy for inflammatory bowel disease: a population-based
study. Gastroenterology 2001; 121(2):255_60.
18. Hommes D, Baert F, van Assche G, Caenepeel F, Vergauwe
P, De Vos M, et al. The ideal management of Crohn's
Disease: top down versus step up strategies, a randomized
controlled trial. Gastroenterology 2006;130:A-108_9 (abstract 749).
19. Best WR, Becktel JM, Singleton JW, Kern F Jr.
Development of a Crohn's disease activity index. National
Cooperative Crohn's Disease Study. Gastroenterology. 1976; 70(3):
439_44.
20. Sandborn WJ, Feagan BG, Hanauer SB, Lochs H, Löfberg
R, Modigliani R, et al. A review of activity indices and
efficacy endpoints for clinical trials of medical therapy in adults
with Crohn´s disease. Gastroenterology. 2002; 122(2):512-30.
21. Dombal FT, Softley A. IOIBD report no. 1: Observer
variation in calculating indices of severity and activity in Crohn's
disease. International Organisation for the Study of
Inflammatory Bowel Disease. Gut. 1987; 28(4): 474_81.
22. Su C, Lichtenstein GR, Krok K, Brensinger CM, Lewis JD.
A meta-analysis of the placebo rates of remission and
response in clinical trials of active Crohn's disease.
Gastroenterology. 2004; 126(5): 1257_69.
23. Fredd S. Standards for approval of new drugs for IBD.
Inflamm Bowel Dis. 1995; 1(4):284_94.
Endereço para correspondência:
Rua San Francisco, 481
Condomínio Débora Cristina
São José do Rio Preto - SP
CEP: 15090-030
jgnetinho@riopreto.com.br
Recebido em 18/11/2008
Aceito para publicação em 07/01/2009
Trabalho realizado na Disciplina de Coloproctologia do Hospital de Base/ Faculdade de Medicina de São José do Rio Preto, SP.